
News information
分类:行业资讯 发布时间:2023-09-12 访问量:739
前 言
抗体药物偶联物又被称为ADC药物,是将细胞毒性分子或药物通过连接子与靶向肿瘤的单抗结合,具有靶向药和化疗药物的特征。
其概念的提出最早可以追溯到100年以前,伴随抗体技术和蛋白质重组工程的进步,越来越多的ADC药物进入临床试验甚至上市。
2019 年至 2022 年间,8 个 ADC 获得 FDA 批准,2022 年,57 个新 ADC 进入 1 期临床试验,与 2021 年相比增加了 90%(图 1)。此外,2022 年启动了 249 项评估 ADC 的临床试验,与 2021 年相比增加了 35%(图2)。
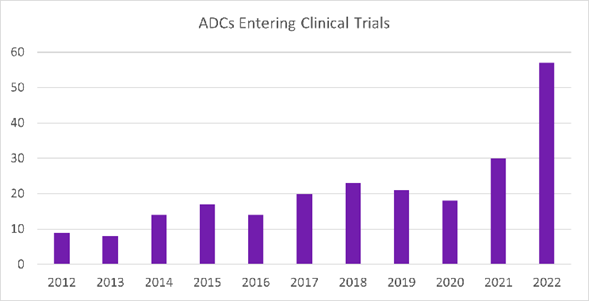
图 1 2012-2022 每年进入临床试验的 ADC产品
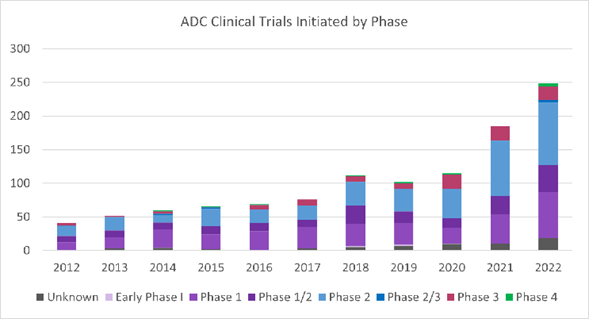
图 2 2012 年-2022每年按阶段分类的 ADC 临床试验
ADC基本原理
抗体-药物偶联物(antibody-drug conjugates, ADCs)通过化学反应,将小分子抗癌药物与重组单克隆抗体(mAb)通过连接子(linker)结合,形成新分子。
ADC需要在最大限度提高效力的同时将非靶标毒性降至最低,因此需要对抗体、连接子和小分子药物以及它们之间的合理组合进行优化,这也是ADC药物设计的核心。
其中,抗体通过与肿瘤细胞表面的抗原结合,精准的将小分子药物递送至肿瘤部位,是影响ADC疗效的核心要素之一。
ADC药物构成及作用机制
药物构成
ADC药物通常包含下述三个关键组成部分:抗体、连接子与小分子细胞毒性药物。
作用机制
ADC药物进入血液后,其抗体成分可以识别靶点并结合到高度表达细胞表面抗原的肿瘤细胞上,当ADC—抗原复合物通过内吞作用进入肿瘤细胞后,该复合物在溶酶体的降解作用下,细胞毒性载荷(药物)会被释放出来,破坏DNA或组织肿瘤细胞分裂,起到杀死肿瘤细胞的作用。
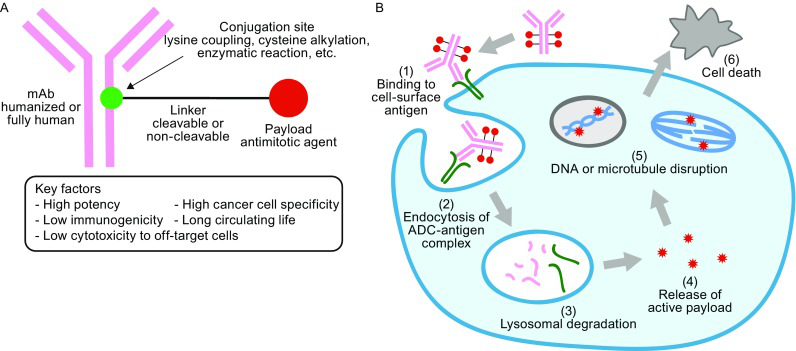
1、靶点/抗原靶点的选择
ADC药物目前主要应用于肿瘤领域,靶点/抗原靶点的选择是设计ADC药物的起点,确定了ADC药物将针对哪些肿瘤适应证,同时潜在影响所偶联的细胞毒药物的选择。
2、细胞毒药物的选择
目前仅有少数几种细胞毒药物及其衍生物用于ADC药物的设计中,主要分为以下两类:微管抑制剂/稳定性破坏剂。
3、连接子的选择
连接子在ADC药物未达到肿瘤细胞之前需足够稳定,否则会产生非预期的毒性。目前在临床应用中的ADC药物所含的连接子主要分为两大类:可裂解的和不可裂解的。
ADC在研药物管线的主流靶点选择
ADC靶向药物选择
靶抗原的选择是ADC药物开发成功的主要因素。靶点是 ADC药物主要识别肿瘤细胞和被内吞的主要媒介,影响药物的成药性和竞争格局。
理想的靶点应具备以下特点:
1.靶点是肿瘤细胞特异性的,不会出现于健康组织细胞;
2.抗原应在配体存在下通过内吞作用内化,并应可再循环至质膜;
3.抗原应是不分泌型的,分泌型抗原可与体内循环系统中的ADC药物或裸抗结合,从而导致与肿瘤细胞结合的 ADC 药物减少,影响药物的疗效和安全性。
目前上市的ADC药物靶点
CD22、CD30、CD33、CD79b、BCMA等5个靶点的适应症为血液瘤;HER2、TROP2、Nectin-4、FRα和TF等靶点的适应症为实体瘤。
关于靶点的可及性,实体瘤相对于血液肿瘤而言,具有更高的阻碍性。实体瘤的微环境等因素导致药物难以渗透,就这一层面而言,血液肿瘤的可及性更好,这也是为什么ADC药物会先在血液肿瘤领域取得突破的关键因素所在。
总 结
ADC药物在乳腺癌、胃癌、尿路上皮癌、肺癌及血液肿瘤等展示出优异的疗效,对比传统治疗方式更加精准、效果更好,为许多癌症提供了一种有希望的治疗方法,让众多癌症患者受益。

国家医保部门从多个方面考虑到参保人员的利益,进而对相关政策进行调整和完善,提升居民的生活幸福感。
2020年-2025年,因新品上市以及患癌人数不断增加,因此从市场规模也随之上升。根据头豹研究院整理,ADC药物的市场规模预计在2024年有望达到74 亿元,2030年预计市场规模达到292亿元人民币,2024-2030年复合增长率为25.71%。

国家卫生健康委发布最新公告显示,2020年各类传播途径的甲乙类传染病发病率均呈现明显下降,其中肠道传染病发病率较2019年下降29.4%、呼吸道传染病发病率较2019年下降12.9%。因此,全球,包括中国在内的抗菌药物的使用额呈下降趋势。
随着新药的不断研发和政策的完善,渐冻症治疗市场有望迎来更加广阔的发展前景。